Hashimoto-Thyreoiditis
Die häufigste Ursache einer latenten Hypothyreose ist die Thyreoiditis Hashimoto. Während ich vor 40 Jahren in meiner Schilddrüsen-Ambulanz nur alle 3 Monate einmal diese Erkrankung sah, haben jetzt ca. 70% meiner Patienten diese Erkrankung, teilweise mit und teilweise ohne Erhöhung der Antikörper gegen Thyreoidea-Peroxidase (Anti-TPO).
Die Thyreoiditis Hashimoto ist keine Erkrankung der Schilddrüse. Die Schilddrüse ist vielmehr das Opfer und Zielorgan eines nicht mehr in der Balance befindlichen Immunsystems. Dieses produziert Antikörper, die gegen die wandständige Thyreoidea-Peroxidase gerichtet sind (Anti-TPO).
Solange diese Antikörper nur in der Schilddrüse wirksam sind, können sie nicht im Blut nachgewiesen werden. Der fehlende Nachweis von Anti-TPO schließt eine derartige Erkrankung also nicht aus. Werden sie aber im Überschuss gebildet, können sie im Blut nachgewiesen werden. Die Erkrankung kann zeitweise ruhen und dann wieder ausflammen.
Bei Aktivierung kann es für einige Zeit zu einer Überfunktion mit entsprechenden Symptomen kommen.In diesem Fall gelangen bereits gebildete Schilddrüsenhormone aus undichten Kolloiddepots in das Blut. Diese Überfunktion limitiert sich selbst, da keine Hormone nachproduziert werden.
Gemeinhin wird angenommen, dass die Diagnose dann gesichert ist. Allerdings gibt es Patienten mit hohen Werten von Anti-TPO, die eine normale Schilddrüsenfunktion haben. Ob diese Patienten behandelt werden sollen, wird von den Thyreodologen (= Ärzte, die sich auf Erkrankungen der Schilddrüse spezialisiert haben,) unterschiedlich beantwortet.

Die Diagnosestellung:
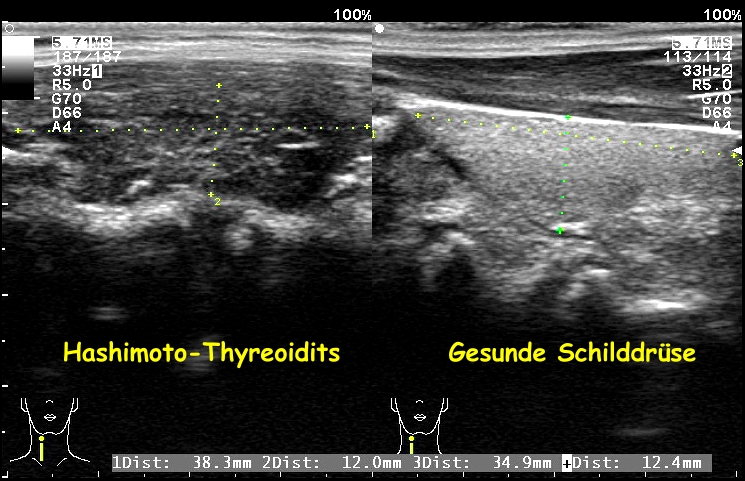
Das früheste Zeichen einer Hashimoto-Thyreoiditis ist ein grobes, echoarmes und häufig auch fleckiges Ultraschall-Muster. Die Veränderungen sind pathognomonisch. Wenn diese ‚typisch‘ sind, dann kann die Diagnose schon bei der Ultraschall-Untersuchung (im Zusammenhang mit den Beschwerden) mit Sicherheit (auch ohne Antikörpernachweis) gestellt werden.
Infektion mit DARS-CoV-2 und einer Hashimotothyreoiditis.
In beiden Fällen ist die Überreaktion des Immunsystems die letzte Ursache.
– Bei der Hashimoto-Thyreoiditis kann man davon ausgehen, dass radikaler Sauerstoff, der bei der Ankoppelung der Jodatome an das Tyrosin-Molekül immer mal wieder ‚abtropft‘ die Threoidea-Peroxidase ‚beschädigt‘. Damit dieser Schaden verhindert wird, existiert eine Glutathion-Peroxidase. Sie fängt dieses Sauerstoffatom ab – allerdings nur, wenn dieser Schutzmechanismus auch effektiv verfügbar ist, was wiederum eine ausreichende Versorgung mit Selen voraussetzt. Im Falle der Schädigung wirkt die Threoidea-Peroxidase ‚fremdartig‘ und kann von einem ‚überstimulierten‘ Immunsystem angegriffen werden. – Die Folgen sind bekannt: Antikörper gegen die Thyreoidea-Peroxidase führen zu einer verminderten Produktion von Schilddrüsenhormonen.
– Im Falle einer Infektion mit SARS-CoV-2 kann es bei einem überstimulierten Immunsystem zu (‚allergischen‘) Entzündungsreaktionen in kleinen Gefäßen kommen. An den entzündlich veränderten Endothelzellen können Gerinnungs-Prozesse intravasal ablaufen mit der Folge von kleinen Thrombosen und – wenn sich diese ablösen und vom Blutstrom verschleppt werden – multiplen (Mikro-)Embolien.
– Ein Immunsystem, das Gefahr läuft, eine Autoimmun-Erkrankung wie die Hashimoto-Thyreoiditis zu entwickeln, könnte also auch bei einer Infektion mit SARS-CoV-2 fehlerhaft reagieren. – Das alleine reicht aber nicht, um einen schweren Krankheitsverlauf zu induzieren. Es müssen noch andere Faktoren hinzutreten: Vorerkrankungen mit verminderter Sauerstoff-Reserve, eine Mikroangiopathie infolge Diabetes oder Hypertonie, ein vorgeschädigtes Endothel bei Arteriosklerose.
Nach neueren Untersuchungen kann CRP ..(hochsensitiv).. neben seiner klassischen Funktion als allgemeiner Entzündungsmarker auch zur Einschätzung des kardiovaskulären Risikos herangezogen werden. Persistierende Werte über 0,3 mg/dl sind demnach als Risikofaktor zu werten (Laborbefundkommentar, Dr. Wisplinghoff).
Ein dauerhaft erhöhter Wert (CRP-hochsensitiv) kann somit auch als Risikomarker für eine Infektion mit SARS-CoV-2 verwendet werden.
– Ein Mangel an Vitamin D begünstigt die Entstehung einer Autoimmunerkrankung. Dies wurde u.a. nachgewiesen bei der multiplen Sklerose, und auch die Hashimoto-Thyreoiditis ist mit einem Vitamin D Mangel assoziiert. – Bei Menschen mit dunkler Hautfarbe, welche in weniger stark beschienen Teilen der Welt leben (z.B. bei Schwarzen in New York) resultiert immer ein Vitamin D Mangel, wenn dieses Vitamin nicht oral zugeführt wird. Hierdurch können die schweren Verläufe erklärt werden. Dies erklärt auch weshalb dunkelhäutige Menschen auf den sonnigen Inseln in Griechenland (Z.B. Migranten auf Lesbos), die keinen Vitamin D Mangel haben, nicht an einer Infektion mit SARS-CoV-2 sterben.